在大多数人类癌症中,耐药性是治疗失败的主要原因。胰腺癌(Pancreatic cancer, PC)是治疗中最具挑战性的恶性肿瘤之一,其特征在于侵袭性强、早期转移和对治疗的高度抗性。患有这种致命性恶性肿瘤的患者平均5年生存率仅为4%。目前,手术切除是唯一可行的治疗方法;然而,80%-85%的PC患者被诊断为晚期疾病,这通常难以完全切除。常规使用细胞毒性治疗来治疗可切除和不可切除的PC病例;然而,只有一小部分患者对治疗有反应,导致总体效益有限,尽管进行了大量研究,但在开发更有效的治疗方法方面进展甚微。吉西他滨(GEM)和基于GEM的化学治疗组合是PC的标准治疗方法,但反应率低(24%),中位总生存时间(5.7个月)增加不多。FOLFIRINOX最近被用作晚期PC患者的治疗选择,中位总生存时间(11个月)略有改善。【注:FOLFIRINOX方案(氟尿嘧啶、亚叶酸、伊立替康和奥沙利铂)已被证实能够延长胰腺癌患者的生存,但不良反应也很严重。】药物抗性被认为是治疗失败的主要原因,这表明迫切需要鉴定和应用预测标志物以将PC患者对应到个体化治疗方案以最小化治疗抗性。
PC的分子和基因组研究表明,对治疗的不同反应可能归因于肿瘤的异质性,这意味着由于克隆多样性,转移可能表现出不同的反应。最近的研究还表明,肿瘤微环境中的细胞-细胞通讯可能参与治疗抵抗。肿瘤来源的外泌体含有蛋白质和核酸,可以作为细胞-细胞通讯的关键介质,增加肿瘤的进展和转移。
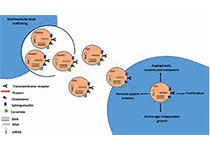
来自美国亚利桑那州立大学的Tony Hu 团队在Theranostics杂志上发表了题为“Chemoresistance Transmission via Exosome-Mediated EphA2 Transferin Pancreatic Cancer”的文章。该研究假设来自化学抗性PC肿瘤的外泌体传递抵抗因子可能增加易感PC克隆的化学抗性。因此,该研究分析了具有可变GEM敏感性的PC细胞系分泌的外泌体,以鉴定可在PC细胞系之间转移GEM抗性的外泌体蛋白。结果表明,Ephrin A型受体2(EphA2)是外泌体介导的GEM抗性转移所必需的。
该研究团队将从耐药胰腺癌细胞上清分泌的exosome分别与两种药物敏感胰腺癌细胞系共孵育。药物毒性试验证实,原本对药物敏感细胞系都分别产生了明显的耐药性,并呈浓度依赖现象。当药物敏感细胞接受来自敏感细胞分泌的exosome后,其对药物的敏感性并没有显着变化。进一步的比较蛋白质组学及相关验证试验证明,耐药的胰腺癌肿瘤细胞分泌的exosome中过表达的EphA2蛋白,其在耐药传递过程中可能起到主要作用。
为了证实exosome携带的Epha2蛋白主导了耐药性的传递的假设,该团队使用小干扰RNA沉默了耐药细胞系的EphA2蛋白在耐药细胞中的表达,并建立了稳定细胞系。吉西他滨药物毒性试验结果证明,耐药细胞系分泌的ExosomeEphA2-失去了传递耐药性给敏感细胞系作用。同时证明exosome是EphA2蛋白的细胞间传递过程中的必要条件。
同时,该研究证实了敏感细胞对exosome的内源化不依赖于EphA2蛋白。针对ExosomeEphA2+和ExosomeEphA2-,敏感细胞都可以将其内源化并表现出相同的效率。使用流式细胞技术的信号结果进一步证实了敏感细胞内源化exosome的含量一致。Western Blot结果则证实被敏感细胞内内源化的EphA2蛋白是伴随加入耐药细胞exosome浓度升高而升高的,但当敏感细胞内源化ExosomeEphA2-后,并没有检测到EphA2蛋白的内源化增加。
对治疗的抵抗导致PC患者的预后不良。存在于肿瘤微环境中的外泌体可以被相邻细胞内化并修饰受体细胞的表型以反映外泌体货物的调节功能。该研究结果表明PC肿瘤外泌体可以传递化学抗性,潜在地允许化学抗性PC细胞将抗性传递到同一肿瘤或其他部位内的敏感PC细胞。发现EXO EphA2表达参与从GEM抗性到GEM敏感性PC细胞的化学抗性转移。
多种蛋白质组学和代谢组学研究试图定义控制PC化学抗性的细胞内通路,但很少有人关注PC衍生外泌体的作用,该结果表明可以通过EphA2依赖性机制转移GEM抗性。大多数先前的报道集中于外泌体介导的影响,以促进而不是转移对化学毒性剂或辐射暴露的抗性,并倾向于鉴定相对非特异性的机制。例如,一项研究提出外泌体可以作为药物输出者起作用以促进化学抗性,发现多柔比星在脱落的囊泡中积累,并且化学抗性与多种细胞系中的囊泡脱落率相关。据报道,从基质细胞到乳腺癌细胞的外泌体转移通过外泌体RNA介导的RIG-I模式识别受体激活促进STAT-1依赖性辐射抗性。很少有研究检测过化学耐药癌细胞外泌体转移耐药性的能力。一项研究提出外泌体介导的从多西他赛耐药的多西紫杉醇敏感乳腺癌细胞的miRNA转移可能通过降低肿瘤抑制蛋白PTEN表达的影响来增强耐药性。该研究结果提供了化学抗性因子的直接外泌体转移的第一个例子,其改变了受体细胞的化学抗性表型。
EphA2过表达并介导乳腺癌、宫颈癌和黑色素瘤的治疗抵抗。最近的研究表明,EphA2的抑制减弱了PC的侵袭性,增加了黑色素瘤对vemurafenib和乳腺癌对他莫昔芬的敏感性,表明EphA2代表了未来癌症治疗的一个有希望的目标。该研究结果揭示了以前未知的富含EphA2的外泌体转移化学抗性的能力。当前迫切需要提高患者对治疗反应的可预测性,以定制治疗并提高总体存活率,特别是对于治疗反应率差导致患者死亡率快的PC患者。尽管在生物标记物开发上付出了巨大努力,但PC治疗的有效预测标记仍然不是很清晰。调节化学抗性的外泌体因子的表征可以作为功能性生物标志物的强有力来源。该研究结果表明,EXO EphA2可能在PC耐药性中发挥重要作用,并暗示分析其他特定外泌体亚群作为PC耐药性的生物标志物可能是有用的。未来的研究需要在具有明确治疗方案的PC患者群体中进行,以验证EXO EphA2的临床效用以及其他潜在的外泌体因子,作为PC耐药性的生物标志物。验证EXO EphA2水平作为PC耐药性的生物标志物将允许受影响的患者被分配到目前正在研究的几种EphA2靶向治疗方案,以提供针对个体治疗的靶向方法。(生物谷Bioon.com)
小编推荐会议
2019(第四届)外泌体与疾病研讨会
http://meeting.bioon.com/2019Exosomes?__token=liaodefeng

尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。