细胞外小泡(EVS)是一种天然的纳米级磷脂双层结构,由真核原核细胞主动释放。20世纪80年代末被发现时,EVS被认为是细胞的“垃圾”,但自那以后研究和方法的发展使研究人员意识到EVS在细胞间通讯中发挥关键作用,通过对免疫功能、组织修复和细胞生长的作用来调节体内平衡和疾病过程。最近的进展显著增加了对EV相互作用和对其受体细胞的影响的了解。

图片来源:https://doi.org/10.1016/j.apsb.2022.05.002
近日,来自四川省医学科学院、四川省人民医院的研究者们在Acta Pharmaceutica Sinica B杂志上发表了题为“Extracellular vesicles: Emerging tools as therapeutic agent carriers”的综述性文章,该研究总结了胞外囊泡可以作为治疗剂载体的新兴工具。
细胞外小泡由真核生物和原核生物分泌,存在于脊椎动物的所有生物体液中,它们通过细胞间的通讯将DNA、RNA、蛋白质、脂质和代谢产物从供体细胞传递到受体细胞。一些EV成分还可以指示其母细胞的类型和生物学状态,并作为液体活组织检查的诊断目标。
EVS还可以通过物理、化学或生物工程策略自然携带或修饰为含有治疗剂(例如,核酸、蛋白质、多糖和小分子)。由于其良好的生物相容性和稳定性,EVS是生物活性成分诱导信号转导、免疫调节或其他治疗作用的理想纳米载体,可以针对特定类型的细胞。
在这里,研究者回顾了EV分类、细胞间通讯、隔离和表征策略,因为它们适用于EV治疗。本文以肿瘤化疗药物、肿瘤疫苗、传染病疫苗、再生医学和基因治疗等领域中具有代表性的实例,对EV作为治疗载体的应用从体外研究到体内动物模型和早期临床应用的最新进展进行综述。最后,研究者讨论了EV疗法目前面临的挑战和未来的发展。
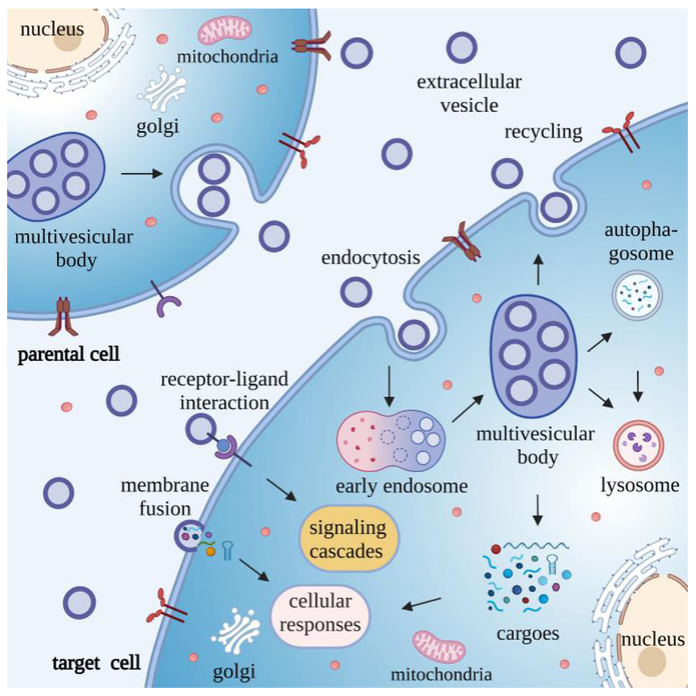
EVS介导的细胞间通讯
图片来源:https://doi.org/10.1016/j.apsb.2022.05.002
不同的载药和表面修饰方法可以影响EV的载药量和完整性,从而改变基于EV的药物释放。因此,优化不同治疗药物的EV加载程序和用于靶向特定细胞和组织靶点的EV修饰方法,以最大限度地提高EV治疗药物在所需部位的生物利用度,并减少治疗剂量和全身副作用,是非常重要的。(生物谷 Bioon.com)
参考文献
Shan Liu et al. Extracellular vesicles: Emerging tools as therapeutic agent carriers. Acta Pharm Sin B. 2022 Oct;12(10):3822-3842. doi: 10.1016/j.apsb.2022.05.002.
尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。