类器官新突破:香港大学周婕/袁国勇团队创立首个双潜能呼吸道类器官培养系统
来源:生物世界
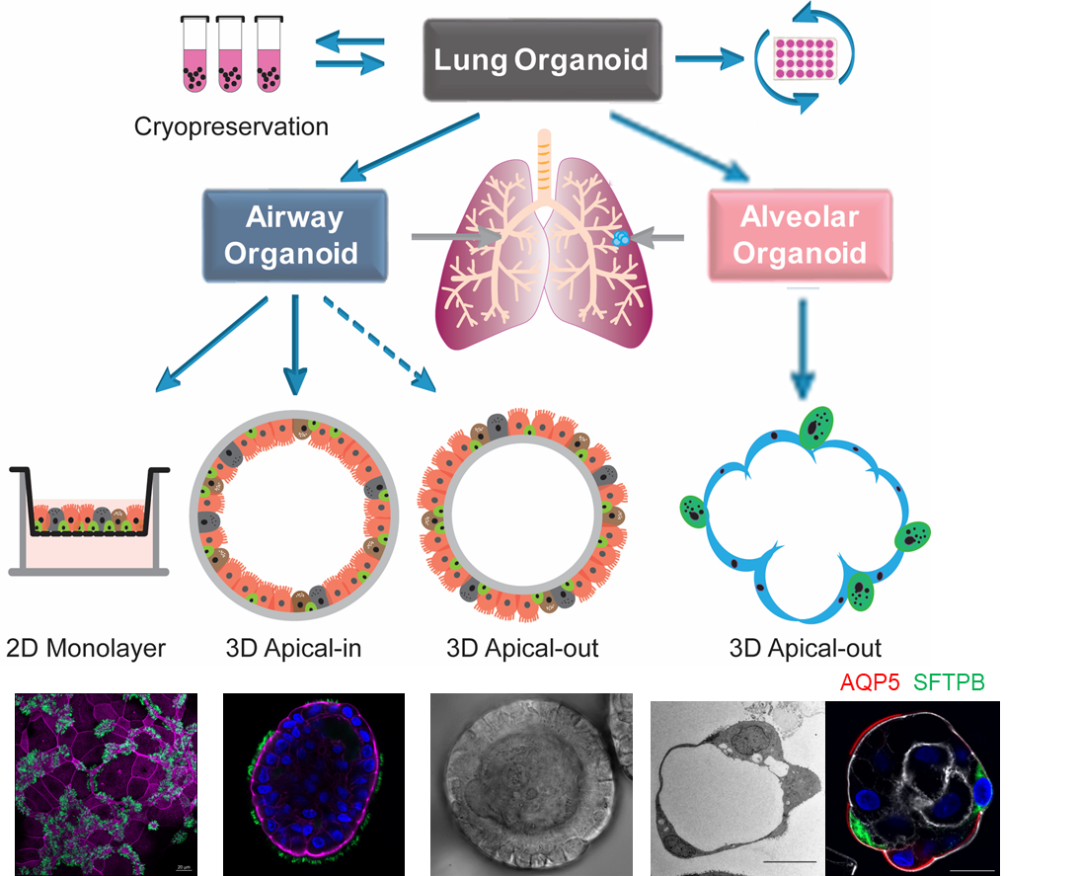
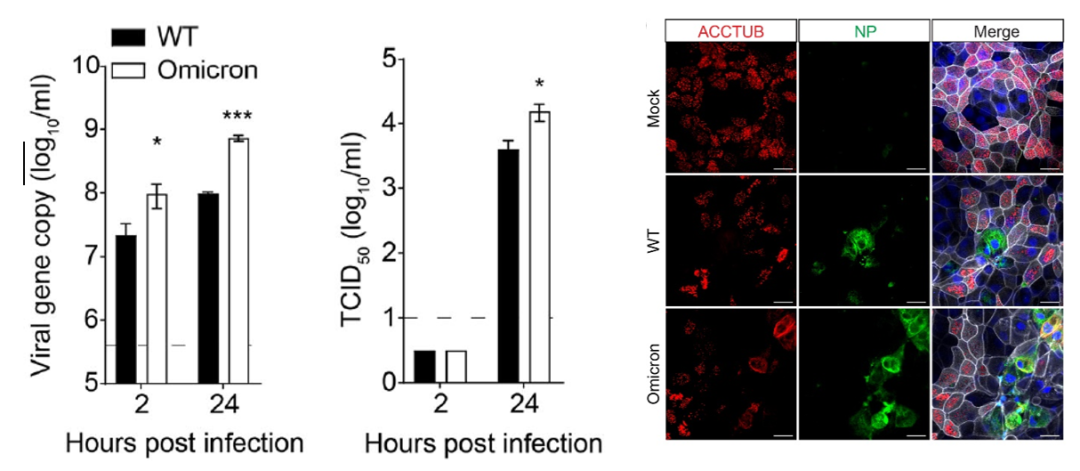
香港大学周婕/袁国勇团队联合类器官先驱 Hans Clevers 及复旦大学姜世勃,在 Cell Discovery 期刊在线发表了题为:A bipotential organoid model of respiratory epithelium recapitulates high infectivity of SARS-CoV-2 Omicron variant 的研究论文。该研究报道了第一个双潜能的呼吸道类器官培养系统,这一培养系统可以将人类的呼吸道上皮在体外长期培养和增殖。人的呼吸道由不断分支的气道和末端的肺泡组成。气道是气体进出肺的通道,肺泡是进行气体交换的功能单位,气道和肺泡分别被覆气道和肺泡上皮。例如新冠病毒主要感染上呼吸道的气道上皮,少数严重的患者会出现下呼吸道或肺泡的感染。2018年,香港大学微生物学系周婕/袁国勇团队与类器官技术创始人、荷兰 Hubrecht Institute 的 Hans Clevers 教授合作,在《美国国家科学院院刊》(PNAS)上发表了题为:Differentiated human airway organoids to assessinfectivity of emerging influenza virus 的研究论文。该研究建立了第一个肺成体干细胞来源的类器官。这些类器官可以连续传代长达一年以上,研究团队在这些持续扩增的类器官中诱导近端分化,建立了可以模拟气道上皮的气道类器官。经过四年的不懈努力,他们又探索出远端分化的方法,建立了可以从形态和功能上模拟肺泡上皮的肺泡类器官。所以,这是一个可以长期扩增的,具有双向分化潜能的呼吸道类器官培养系统(图1)。2020年初,在新冠病毒爆发期间,周婕/袁国勇团队在 Nature Medicine 期刊发表了题为:Infection of bat and human intestinal organoids by SARS-CoV-2 的研究论文。该研究建立了第一个蝙蝠肠类器官培养,在蝙蝠和人类肠道类器官中进行的研究提供了第一个实验证据,表明新冠病毒起源于蝙蝠。在这篇最新的 Cell Discovery 论文中,研究团队进一步优化了已有的气道类器官,优化的气道类器官展示出 Omicron 变异病毒株更高的感染性(图2)。总的来说,香港大学微生物团队建立的呼吸道上皮类器官培养系统提供了一个功能强大的、具有生物活性的研究工具,使得科学家可以将呼吸道的生理和疾病在培养皿中进行,代表着这一研究领域一个重大突破。复旦大学基础医学院的姜世勃教授,荷兰 Hubrecht Institute 的 Hans Clevers 教授,港大微生物学系袁国勇教授和周婕博士为论文的通讯作者,香港大学微生物学系博士研究生赵文俊和刘晓娟,以及研究助理教授李存博士为论文的共同第一作者。该研究获得香港政府大学教育资助委员会和创新科技署的资助。