多发性硬化(MS)是中枢神经系统最常见的炎性脱髓鞘性疾病,可分为复发缓解型(复发后缓解,每次发作均基本恢复)和进展型(疾病进行性加重)。
现有的治疗方式对于复发缓解型MS效果较好,但进展型MS(PMS)仍缺乏有效的治疗方式[1]。
近日,来自意大利圣拉斐尔科学研究所的Gianvito Martino团队,在《自然·医学》杂志发表了首个评估鞘内移植人胎儿神经前体细胞(hfNPC)治疗PMS的可行性、安全性和耐受性的1期临床试验结果[2]
经过2年的随访,研究人员未发现与hfNPC移植相关的严重不良反应。此外,探索性疗效分析显示,接受最高剂量hfNPC移植治疗的患者脑萎缩发生率较低,且脑脊液中抗炎和神经保护因子的水平较高。
这些结果表明hfNPC移植治疗PMS患者具有较高的可行性和安全性,且可能起到一定的治疗效果,值得在未来更大的队列中进一步评估hfNPC移植治疗PMS的有效性。

论文首页截图
在MS动物模型中,研究人员已证明了移植的神经前体细胞可以分化为成熟的神经细胞,并释放相关细胞因子发挥营养支持和抗炎功能,从而减少脑内脱髓鞘病变、星形胶质细胞增生和轴突损伤[3, 4]。
在此基础上,Gianvito Martino团队开展了前瞻性、开放标签、剂量探索(3+3设计)的1期临床研究(STEMS,NCT03269071,EudraCT2016-002020-86),初步评估了hfNPC移植治疗PMS的可行性和安全性。
研究的主要纳入标准为:年龄在18-55岁,根据修订版McDonald 2010标准和2013 Lublin分型诊断为PMS,且对所有经批准疗法无效/不耐受。
被纳入研究的受试者将通过腰椎穿刺接受鞘内注射hfNPC(由流产的10-12周人胎儿获得),hfNPC的剂量递增分为4档:TC-A,0.7×106/kg;TC-B,1.4×106/kg;TC-C 2.8×106/kg和TC-D 5.7×106/kg。在完成治疗后,将对受试者进行为期96周的随访。研究的主要终点为鞘内注射hfNPC的可行性、安全性和耐受性。
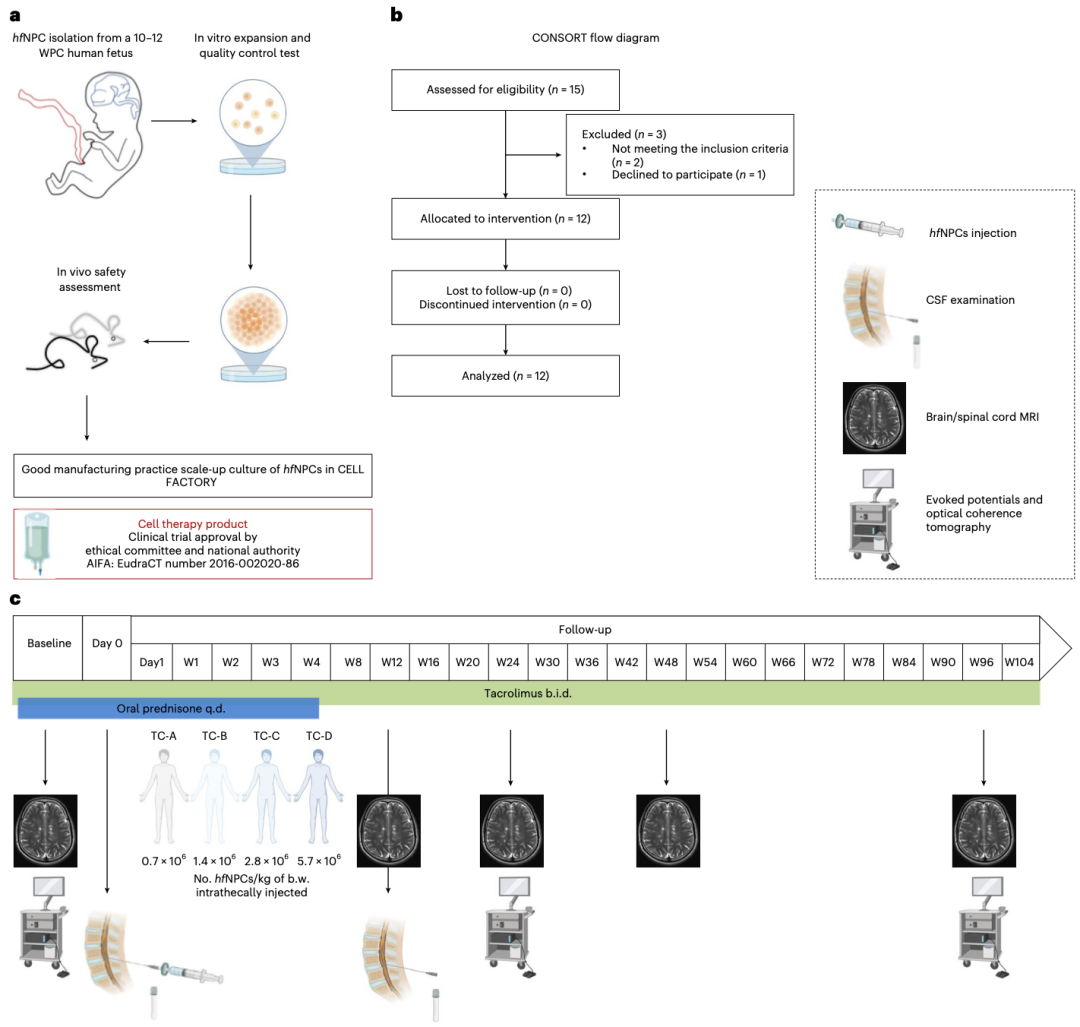
研究流程图
在2017年5月至2019年5月间,共有15名PMS受试者入选,其中12名受试者最终接受了hfNPC移植治疗,2名受试者因禁忌症(无法接受免疫抑制治疗)而退出试验,1名受试者在hfNPC移植前自发退出试验,末次随访时间为2021年6月。
总体来说,受试者对hfNPC移植治疗的耐受性良好,在接近两年的随访内观察到的不良反应大多为1级或2级,且不同治疗剂量之间不良反应的发生率无明显差异,也没有观察到剂量限制毒性(DLT)。
在整个研究期间,未观察到与hfNPC移植治疗相关的严重不良反应(3级或更高),也没有任何明确的与hfNPC移植治疗相关的不良反应。截止末次随访,患者的存活率为100%。
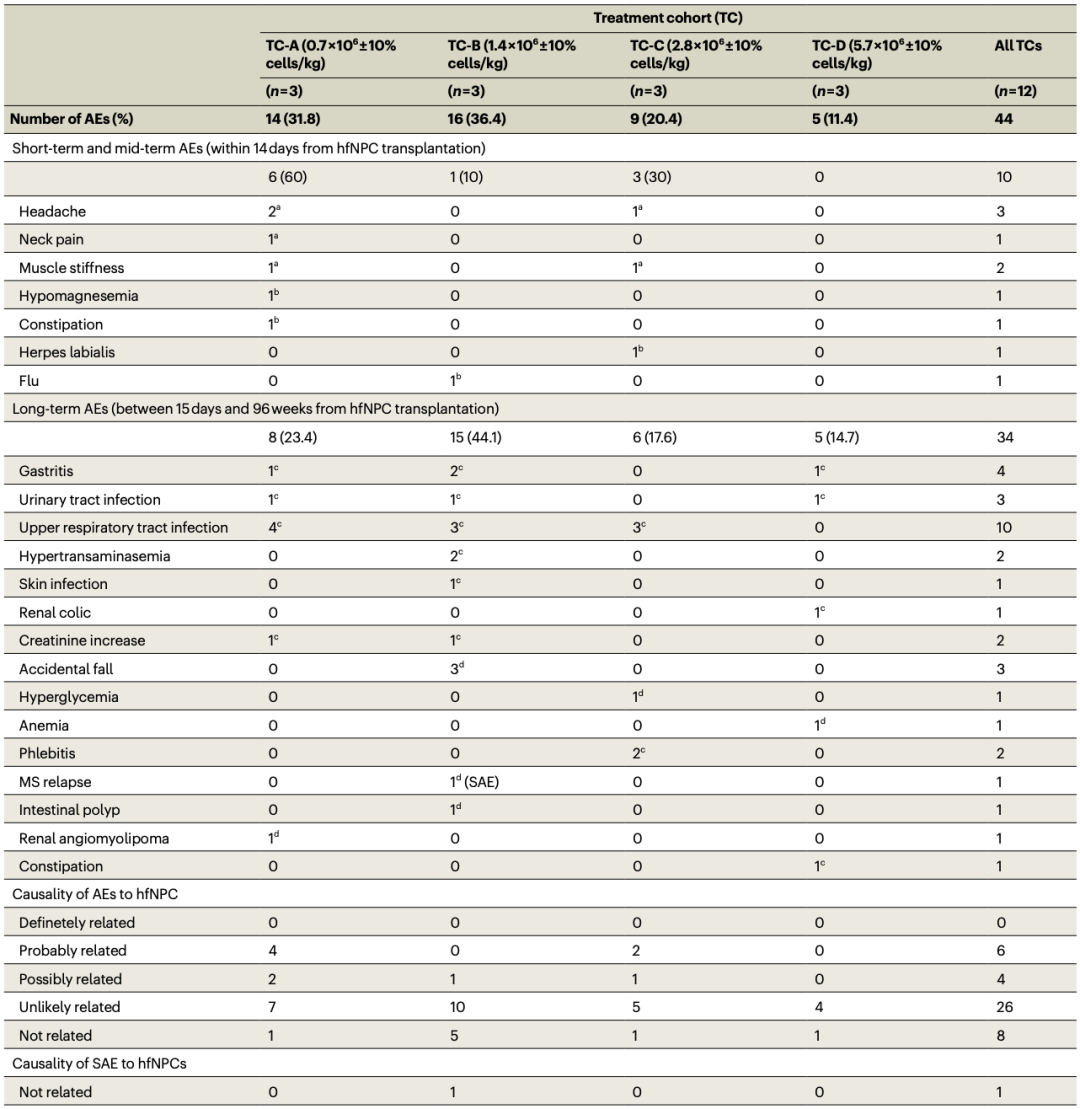
研究中出现的不良反应
紧接着,研究人员探索了hfNPC移植治疗的效果。
在移植治疗的前4年,受试者的临床扩展致残量表评分(EDSS)平均每年增加0.24分,在接受移植治疗的2年内,受试者的EDSS平均每年增加0.13分,虽然相比于移植治疗前,MS的进展变缓慢,但两者无明显统计学差异。
同时,其他的临床评分(9-HPT评分和SDMT评分)以及神经生理学评估结果(如运动诱发电位、感觉诱发电位和周围视网膜神经纤维层厚度)在治疗前后也无明显差异,且与hfNPC的治疗剂量无明显相关性。
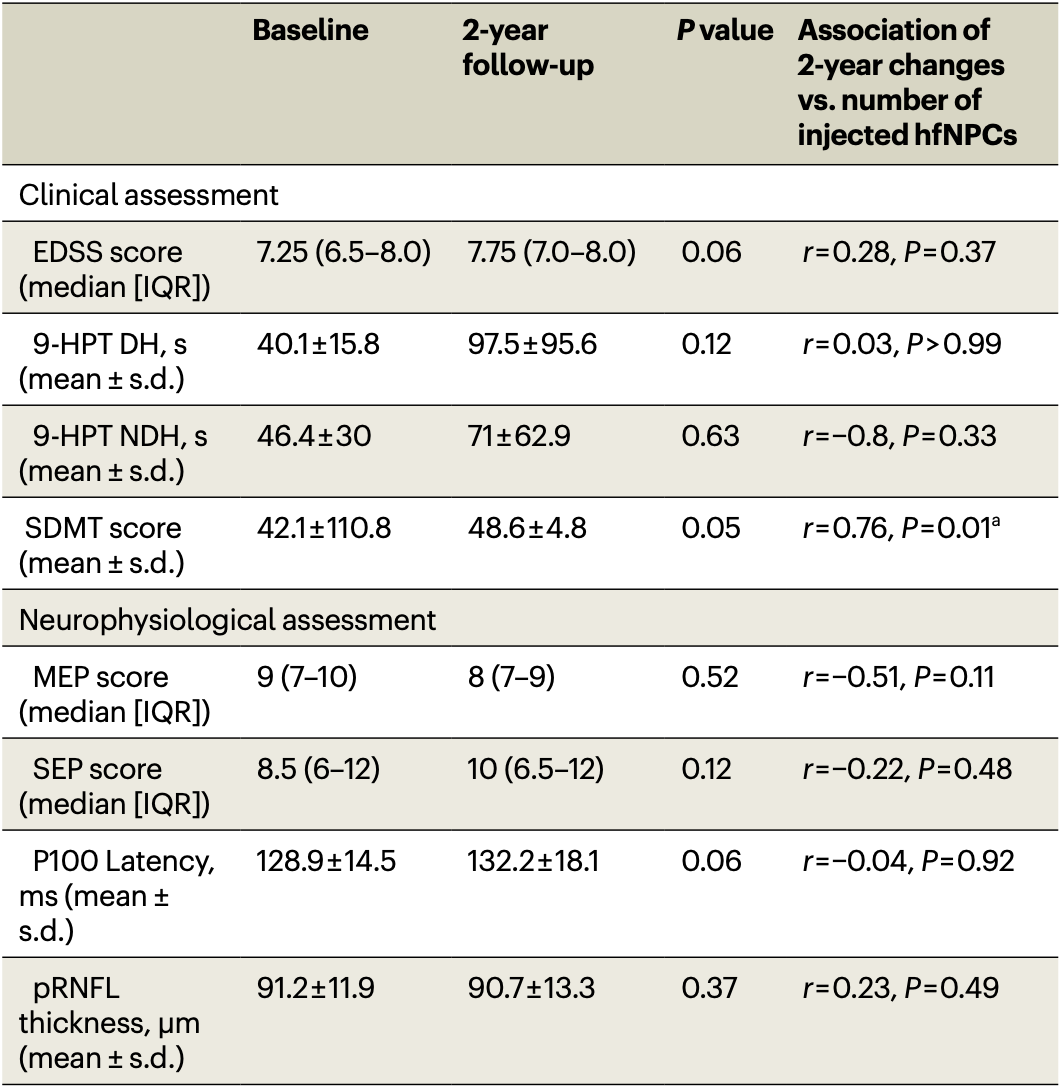
受试者神经功能和神经生理学评估结果
磁共振成像(MRI)评估显示,6例(50%)受试者在随访期内出现新的T2病变(T2病变体积增加1.1±0.82 ml/年,3例病变增强扫描出现强化),hfNPC移植剂量与新的T2病变数目、体积以及增强扫描强化数目均无明显相关性。
值得注意的是,hfNPC低剂量组和高剂量组受试者的灰质萎缩速度差异具有统计学意义(P=0.04),接受低剂量hfNPC移植治疗的受试者在移植后2年内脑萎缩快于高剂量组。无论是总脑体积,还是灰质、白质体积,萎缩的速率均与hfNPC的剂量呈负相关。
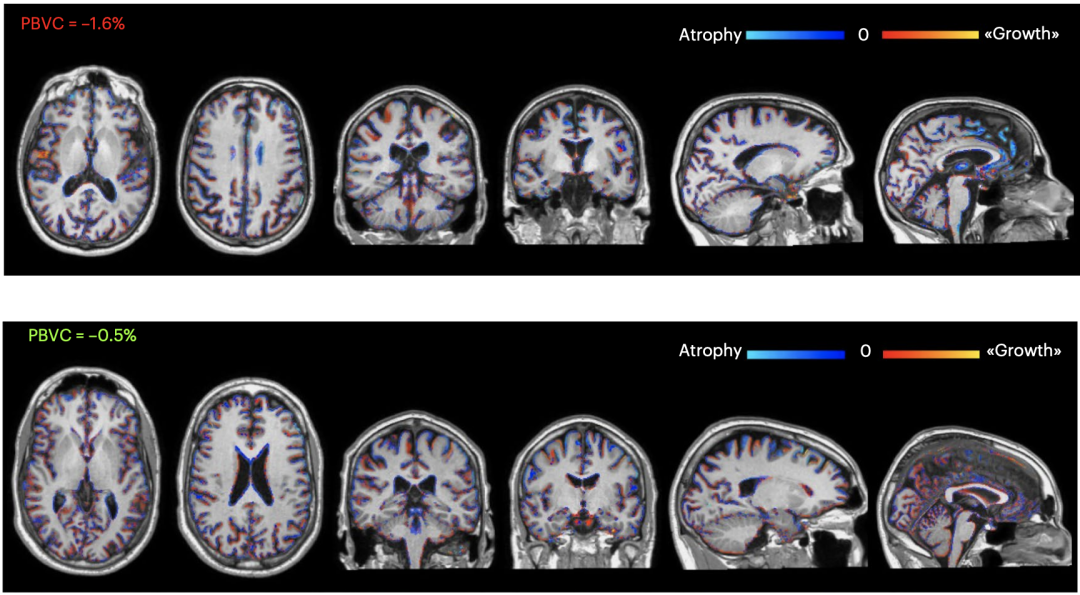
低剂量(上图)hfNPC移植治疗的受试者在移植后2年内脑萎缩显著快于高剂量组(下图)
接下来,研究人员对受试者的脑脊液成分进行了分析。
在移植后3个月,受试者脑脊液中细胞数量和蛋白质明显增加,hfNPC移植剂量与脑脊液蛋白水平呈正比(P=0.06),而与细胞数量无明显相关性。从5个受试者脑脊液中可提取到足够的DNA进行分析,其中1个受试者脑脊液中可检测到供体来源细胞DNA的存在。
最后,研究人员对受试者脑脊液进行了组学分析。
在检测的46种细胞因子、趋化因子和生长因子中,有17种在基线和移植后均低于可检测的范围(CCL4、CCL11、EGF、G-CSF、IFN-y、IL-1b、IL-5、IL-7、IL-12p40、IL-12p70、IL-17、IL-22、LIF、PDGF-AB、PDGF-BB、RANTES和TGF-B)。
对所有在基线和移植后3个月可检测到的因子进行主成分分析发现,相比于低剂量移植组,高剂量组在移植后各因子的变化程度更大。
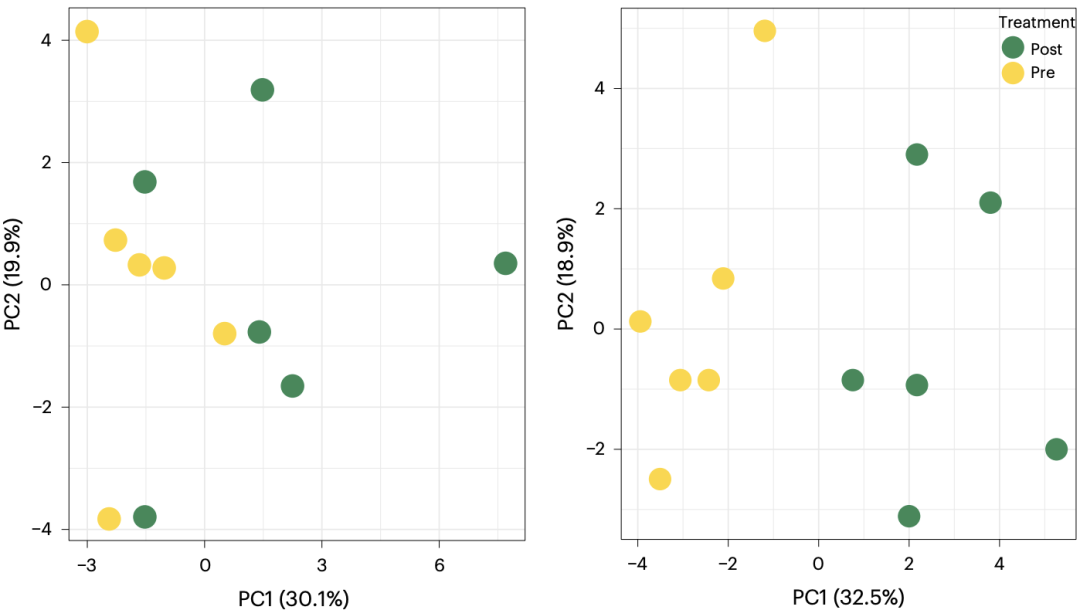
低剂量组(左)和高剂量组(右)在移植前后细胞因子主成分分析
在hfNPC移植后,血管生成素-2、CCL-2、CXCL10、FAS配体、GDNF、GM-CSF、IL-10、IL-15、IL-2、MMP9、SCF、TNF-β和VEGF-C(营养因子和免疫相关因子)显著升高,而IL-8水平(促炎)显著下降。
脑脊液的蛋白质组学分析也显示,hfNPC移植后脑脊液蛋白质图谱发生了变化。在低剂量组和高剂量组中检测到的707和714个蛋白质中,分别有63种和78种蛋白质在基线和移植后3个月的脑脊液中存在显著差异(P<0.05)。
这些差异蛋白的基因本体论(GO)分析显示,细胞外基质聚集、细胞迁移和粘附、轴突发育等通路,在低剂量组和高剂量组中均明显富集;此外,低剂量组中还有免疫系统、固有免疫系统和中性粒细胞脱颗粒等通路明显富集(高剂量组未富集),而高剂量组中则是神经元投射形态发生、细胞对生长因子的反应和突触聚集等通路明显富集(低剂量组未富集)。
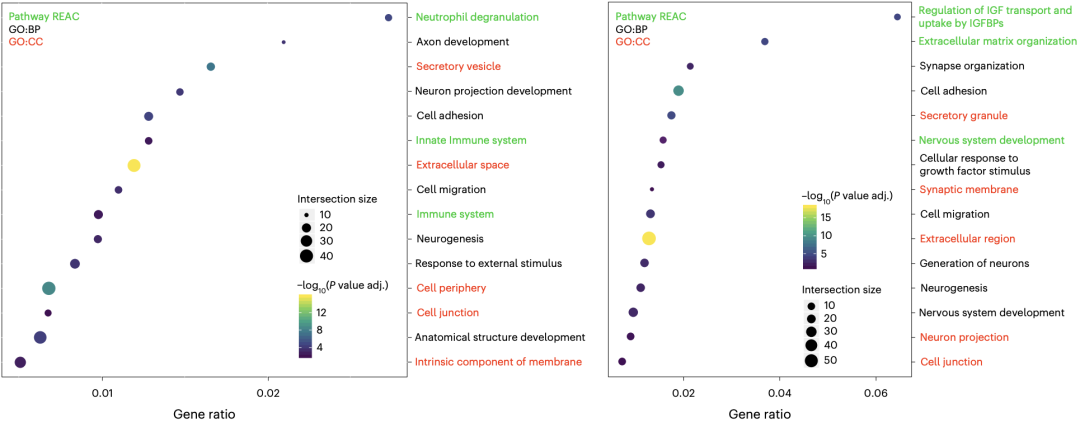
低剂量(左图)和高剂量(右图)组治疗前后差异蛋白的GO分析
为了更详细地研究脑脊液蛋白质组的变化,研究人员进行了基因集合富集分析(GSEA)。该分析显示,在hfNPC移植后,与固有免疫相关的通路总体上呈下调趋势(中性粒细胞脱颗粒、免疫系统、固有免疫系统),而参与神经系统发育、神经发生和细胞迁移的通路总体上呈上调趋势。
总的来说,STEMS是首个评估PMS患者鞘内移植hfNPC治疗安全性和最大耐受剂量的临床试验,并证明了该疗法的可行性和安全性。
更为重要的事,探索性疗效分析显示hfNPC移植疗法可减缓患者的脑萎缩,且增加脑脊液内抗炎和神经保护因子的水平,值得进行下一阶段的临床研究。
参考文献
1.The Lancet N: Multiple sclerosis under the spotlight. Lancet Neurol 2021, 20(7):497.
2.Genchi A, Brambilla E, Sangalli F, Radaelli M, Bacigaluppi M, Furlan R, Andolfo A, Drago D, Magagnotti C, Scotti GM et al: Neural stem cell transplantation in patients with progressive multiple sclerosis: an open-label, phase 1 study. Nat Med 2023.
3.Pluchino S, Quattrini A, Brambilla E, Gritti A, Salani G, Dina G, Galli R, Del Carro U, Amadio S, Bergami A et al: Injection of adult neurospheres induces recovery in a chronic model of multiple sclerosis. Nature 2003, 422(6933):688-694.
4.Pluchino S, Gritti A, Blezer E, Amadio S, Brambilla E, Borsellino G, Cossetti C, Del Carro U, Comi G, t Hart B et al: Human neural stem cells ameliorate autoimmune encephalomyelitis in non-human primates. Ann Neurol 2009, 66(3):343-354.
尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。