许多已知的致癌基因并不是一个好的药物靶点,这可能由很多原因导致,比如说没有理想的小分子结合部位,或者药物可能同时抑制与其相似的其它蛋白的功能而导致副作用。其中一个很好的例子就是胰腺癌中常见的KRAS突变基因。胰腺癌是一种非常凶险的癌症,死亡率极高,但是又没有有效的药物。研究显示超过90%的胰腺癌带有KRAS突变,KRAS突变不仅能引发癌症,还能加速肿瘤生长和转移。
令人遗憾的是,KRAS蛋白是一个“不可成药”的靶点,许多寻找靶向药物的尝试都失败了。近来RNA干扰(RNAi)技术的发展给癌症靶向治疗又带来的新希望。使用小分子RNA可以选择性地阻止致癌基因的表达,同时又不影响正常基因的功能,理论上是一种理想的靶向治疗方法。不过,由于RNA分子的高度不稳定性,如何将RNA送到肿瘤是一个新难题。研究者尝试了病毒、脂质体、纳米颗粒都多种手段,却遭遇了运送效率低,以及引起免疫反应导致载体被清除出系统等问题。
最近,来自美国得克萨斯州安德森癌症中心(MD Anderson Cancer Center)的科学家们发明了一种新的运送RNAi的方法,这种方法利用了一种细胞天然产生的囊泡,称之为外泌体(exosome)。通过外泌体成功地将针对KRAS突变的RNAi分子送到了肿瘤细胞中,并在小鼠模型中取得了很好的抗癌效果。这项研究发表在了最近的《自然》杂志上。
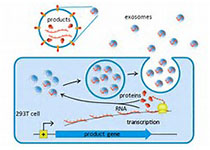
人体中几乎所有的细胞都会分泌和吸收只有几纳米大小的外泌体。外泌体在所有的体液中都能被发现,据估计,人体中外泌体的数量是细胞数量的1000倍。外泌体可以在细胞之间运送各种生物大分子,诸如DNA、RNA、蛋白质和脂质等,这是细胞之间互相联系的一种手段。外泌体根据其表面不同的蛋白,能够靶向不同的细胞,因此是一种理想运送药物的载体。
在这项研究中,美国科学家们首先发现外泌体上表达的CD47蛋白能够发出“不要吃我”的信号,有效抑制循环系统中的单核细胞对分泌体的吞噬作用。他们通过基因工程专门制造了带有CD47的外泌体,使得外泌体在循环系统中能够存在更长的时间,大大提高了运送药物的效率。随后他们发现,KRAS突变使得胰腺癌细胞的巨胞饮作用增强,增强的巨胞饮作用恰好加快了癌细胞接受外泌体的速度,同时CD47的存在不会影响巨胞饮作用。这一现象使得运送药物的外泌体更易被癌细胞吸收,从而降低了其产生副作用的可能。
基于这两项发现,科研人员生产了一种被命名为iExosome的外泌体,它表面带有CD47,内含针对KRAS G12D突变的小干扰RNA(siRNA)或短发卡RNA(shRNA)分子。在两种不同的胰腺癌小鼠模型,包括PANC-1细胞异体移植模型和带KRAS突变的小鼠中的研究发现,iExosome将小RNA分子送入了肿瘤细胞,有效地抑制了肿瘤的生长。接受iExosome治疗的小鼠在200天后的平均生存率超过80%,而没有接受治疗的小鼠在200天的存活率为0%。
这项来自于安德森癌症中心Raghu Kalluri博士实验室的基于外泌体的技术平台,以及iExosome这个针对KRAS突变胰腺癌的候选药物,已经授权给了位于美国马萨诸塞州剑桥的新创生物技术公司Codiak Biosciences。Codiak在2015年由ARCH Venture和Flagship Pioneeing等多家投资机构联合创建,致力于开发基于外泌体的新药。
Codiak总裁兼首席执行官Douglas Williams博士表示:“Kalluri博士团队发表的这项研究突出展示了外泌体作为治疗方式的潜力。成功靶向KRAS突变并在胰腺癌小鼠模型中看到的强大疗效只是其中的一个例子。Codiak正在继续拓展这些重要的发现。“
我们希望外泌体研究继续迅速发展,早日为胰腺癌和其它疾病患者带来新药。(生物谷Bioon.com)

尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。